
 대한민국 미래 먹거리 분야로 꼽히는 '바이오'. 최첨단 기술이 접목돼 허가 난이도는 높고, 신속한 심사가 필요하지만 규제기관 내 허가부서가 임시조직에 불과해 정규 직제 전환을 요구하는 목소리가 나오고 있다.
대한민국 미래 먹거리 분야로 꼽히는 '바이오'. 최첨단 기술이 접목돼 허가 난이도는 높고, 신속한 심사가 필요하지만 규제기관 내 허가부서가 임시조직에 불과해 정규 직제 전환을 요구하는 목소리가 나오고 있다.
최근 국정기획위원회의 '대한민국 진짜 성장을 위한 전략' 정책 해설 보고서에 따르면 이재명 정부는 현재 11위인 국내 바이오헬스케어 산업을 글로벌 7위로 키운다는 구상을 내놓았다.
2023년 기준으로 한국 바이오 시장 규모는 2160억달러(1.6%)로 11위다. 7위 캐나다는 3000억달러(2.2%) 수준으로 격차가 크지 않다.
산업 성장을 통해 한국보다 앞서 있는 호주, 브라질, 이탈리아, 캐나다를 제치고 글로벌 7위 국가가 되는 것을 목표로 잡았다.
이를 위해 산업계 역할은 물론 규제기관 지원도 필수다. 첨단제품 상용화를 위해 새로운 허가기준 및 절차를 마련하고 신속 허가를 담당할 조직 및 인력을 갖춰야 한다.
현재 국내 식품의약품안전처에서 바이오의약품 허가 관련 업무는 '바이오허가TF'가 총괄하고 있다. 지난해 차장 직속 '허가총괄담당관'을 폐지하면서, 바이오생약국 내 TF 형태로 재배치됐다.
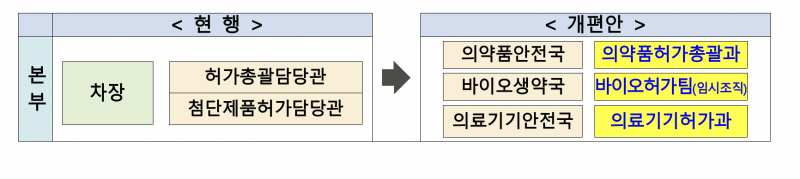
의약품과 의료기기의 경우 허가 담당 부서가 정규 직제로 편성됐지만, 바이오의약품은 허가 건수가 상대적으로 적다는 이유로 임시조직으로 편성됐다.
자연히 조직 규모 또한 적다. 의약품허가총괄과의 경우 17명으로 구성돼 있지만, 바이오허가TF는 7명에 불과하다. 이들이 연간 50여 건의 바이오의약품 허가 업무를 담당하고 있다.
바이오생약국 관계자는 "아직 국내 바이오 비중이 낮아 의약품과 의료기기와 달리 바이오허가부서는 TF로 머물러 있다"며 "첨단 기술이 많고, 시장 진입 속도가 중요한 만큼 개선이 필요하다"고 말했다.
 ''. , .
''. , .
' ' 11 7 .
2023 2160(1.6%) 11. 7 3000(2.2%) .
, , , 7 .
. .
'TF' . '' , TF .

, .
. 17 , TF 7 . 50 .
" TF " " , " .

