[데일리메디 양보혜 기자] 한미약품이 개발한 항암신약의 상용화 개발을 진행 중인 파트너사들이 지난 4일부터 온라인으로 개최된 2021 미국임상종양학회(ASCO)에서 주요 임상 연구결과를 구연 및 포스터로 발표했다.
◆ 스펙트럼, 뇌(腦) 전이서 포지오티닙 유효성 결과 공개
파트너사 스펙트럼은 EGFR 또는 HER2 Exon20 돌연변이를 가진 비소세포폐암(NSCLC) 환자에서 포지오티닙의 중추신경계(CNS) 활동에 대한 결과를 포스터로 발표했다.
발표된 ZENITH20 임상은 EGFR과 HER2 Exon20 삽입 비소세포폐암 환자를 모집한 글로벌 임상으로, 코호트 1, 2와 3에서 총 284명 환자 중 뇌전이를 가진 36명의 결과를 평가했다.
평가된 36명의 환자들은 초기모집 단계(Baseline)부터 독립적인 연구소에서 검증한 전이 뇌종양을 가지고 있었으며, 이중 8%인 3명에서 완전관해(CR)를 보였다.
뇌 종양은 비소세포폐암 환자 가운데 최고 25%에서 발생하는 흔한 전이로, 짧은 생존기간과 관련이 있다. 환자들은 포지오티닙 16mg을 1일 1회 투여받았다.
스펙트럼 최고의학책임자 프랑수아 레벨은 “중추신경계(CNS) 전이는 비소세포폐암 환자에서 흔하고 생명을 위협하는 합병증”이라며 “이번 데이터는 EGFR 혹은 HER2 Exon 20 삽입 돌연변이를 가진 중추신경계(CNS) 전이 환자에서 포지오티닙의 의미있는 임상적 치료 유용성을 보여준다”고 말했다.
◆ 벨바라페닙, 흑색종 환자서 병용요법 및 용량 결정 임상 진행
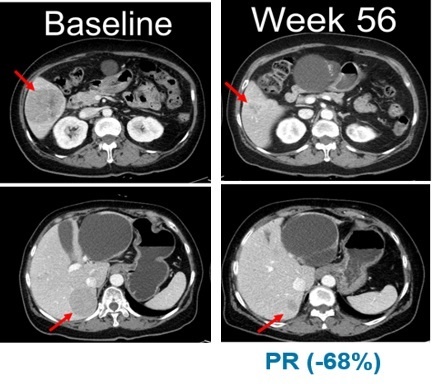
또 다른 파트너사 제넨텍은 진행성 고형암 환자를 대상으로 ‘벨바라페닙’과 코비메티닙 병용요법을 진행한 연구 결과를 구연으로 발표했다.
벨바라페닙은 한미약품이 2015년 로슈 자회사 제넨텍에 라이선스 아웃한 항암 혁신신약 후보물질로, 이번 국내 연구에서 벨바라페닙의 신규 용량에서 내약성 및 안전성을 확인했다.
벨바라페닙은 강력한 선택적 RAF 이합체 억제제로, RAF와 RAS 변이로 인한 고형암에서 항종양 효과를 나타낸다. 이번 발표는 벨바라페닙의 HM-RAFI-103 연구로, 연세암병원 종양내과 신상준 교수가 진행했다.
이번 임상은 BRAF, NRAS 변이 고형암 환자에 '벨바라페닙'과 '코비메티닙'을 병용투여한 1b상 연구로 용량 증량과 적응증 확장, 두 단계로 나뉜 임상이다.
1차 평가변수로는 안전성과 내약성, 최대 내약용량(MTD) 및 임상2상 권장용량(RP2D)을, 2차 평가변수로는 약동학과 약력학, 항종양효과를 확인하는 것으로 연구가 진행됐다.
적응증 확장 임상의 NRAS 변이 흑색종 연구에서는 환자 13명 중 5명이 부분반응(PR)을 보였으며, 최고반응률(BORR)은 38.5%로 나타났다.
13명 중 11명은 이전에 면역관문억제제(CPI)를 투여 받았으며, 면역관문억제제 투여 환자군 대상 최고반응률(BORR)은 45.5%로 확인됐다. 무진행생존기간(PFS)의 중간값은 7.3개월이다.
총 19명의 환자가 용량 증량 코호트에 등록됐고, 벨바라페닙 200mg 1일 2회(BID)와 코비메티닙 40mg 1일 1회(QD) 용량을 투여한 3명 중 2명에서 각각 3단계의 대장염, 설사, 매스꺼움 증상이 나타났다.
하지만 벨바라페닙을 300mg 1일 2회(BID)까지 증량 투여 하고 코비메티닙 20mg 1일 1회(QD)로 감량했을 때, 용량제한독성(DLTs)은 나타나지 않았다.
이번 발표를 진행한 신상준 교수는 “이번 연구를 통해 벨바라페닙의 우수한 안전성 및 항암효과를 확인했다”며 ”특히 NRAS 유전자 돌연변이를 지닌 흑색종 환자에서 고무적인 효과를 확인할 수 있었다”고 말했다.
◆ 오라스커버리 플랫폼 적용한 오라독셀 최초 발표
아테넥스는 한미약품이 개발한 플랫폼 기술 ‘오라스커버리(ORASCOVERY)’를 적용해 도세탁셀 항암제를 경구용으로 전환환 오라독셀(도세탁셀+엔서퀴다) 약동학 연구 임상 1상을 발표했다.
이어 정맥주사용 항암제 파클리탁셀을 경구용으로 전환한 오락솔의 분자아형(Molecular subtype)에 따른 항암효과를 분석한 임상 3상 추가 하위분석 데이터 2건을 각각 포스터로 발표했다.
아테넥스는 정맥주사요법(IV) 대비 오라독셀 생체 이용률, 안전성 및 내약성을 결정하기 위한 오픈라벨, 양방행 교차(Two-way crossover) 설계 약동학 연구 1상을 진행했다.
오라독셀 투여 시 용량 제한 독성 또는 약물 관련 심각한 부작용은 없었다. 또, 평균 절대적 생체 이용률은 15.9% 였으며, 300 mg/m2 용량에서 약동학(PK)이 비선형(non-linear)으로 나타났다.
이번 임상 결과와 관련된 연구를 바탕으로 아테넥스는 오라독셀 300 mg/m2 용량 분할에 대해 추가적인 평가를 진행하고 있다.
또한 전이성 유방암(MBC) 환자 대상 분자아형에 따른 항암효과 임상 3상 사후분석 연구을 보면 총 402명의 무작위 배정 환자를 포함한 치료의향 모집단(ITT)에서의 오락솔의 객관적반응률(ORR)은 35.8%로 23.4%를 보인 파클리탁셀 정맥주사요법(IV) 보다 우월했다.
이외에도 HR양성/HER2음성 등 총 4개의 분자아형 그룹 모두에서 오락솔이 정맥주사요법(IV) 대비 객관적반응률(ORR)이 높았다.
한미약품 권세창 사장은 “우리와 긴밀한 연구협력을 맺고 있는 파트너사들이 세계 최대 규모 암학회에서 개발 중인 혁신신약의 유효한 결과를 발표하게 돼 기쁘다”며 “최근 네이처지에 벨바라페닙 연구결과가 등재되는 등 글로벌 학계에서도 한미약품 개발 혁신신약을 주목하고 있다”고 말했다.
 또 다른 파트너사 제넨텍은 진행성 고형암 환자를 대상으로 ‘벨바라페닙’과 코비메티닙 병용요법을 진행한 연구 결과를 구연으로 발표했다.
또 다른 파트너사 제넨텍은 진행성 고형암 환자를 대상으로 ‘벨바라페닙’과 코비메티닙 병용요법을 진행한 연구 결과를 구연으로 발표했다. 